

众所周知,现有基因在复制和修饰的过程中将有可能产生新蛋白质编码基因(new protein-coding genes);然而近几年的研究发现,从头起源(de novoorigination)同样在新基因的产生中发挥着重要作用:在这一模型下,新基因从人类祖先的非编码DNA区域横空出世,形成前所未有的编码蛋白。
然而,这些新基因是如何从非编码区域逐步产生的呢?北京大学未来技术学院李川昀教授课题组运用恒河猴作为人类近缘物种的优势,发现lncRNA(长非编码RNA)可能是新蛋白编码基因(new protein-coding genes)诞生的前体。相关研究结果以题为 “De novo genes with an lncRNA origin encode unique human brain developmental functionality ”的长文形式在Nature Ecology & Evolution 杂志(IF: 19.1)在线发表。

https://www.nature.com/articles/s41559-022-01925-6
“所见即有功能”是如何实现的?
01
李川昀团队与中国科学院动物研究所胡宝洋教授团队合作,揭示U1等顺式元件介导的RNA出核是区分mRNA(蛋白编码基因产物)和lncRNA(非编码基因转录产物)的核心屏障;而自然选择通过控制发生在这些核心元件上的突变,维持两类RNA分子在核、质定位上的界限。在偶然情况下,某些发生在lncRNA基因上的突变,可以促进这些lncRNA出核并翻译,而仅当翻译出的蛋白对于该物种具有适应性的新功能时,这些突变被固定,从而促成一个全新的蛋白编码基因----这些新基因就像成功的“偷渡者”一样,由于其具备新的适应性功能,因此成功地跨越了两类分子之间的界限,进而表现出“起源即有功能”的预适应特征(preadaptation)。
进一步地,研究者结合人源类脑器官模型和转基因小鼠模型,对一例以上述模式起源的新基因开展了功能研究,揭示了该基因在促进人脑增大等人类适应性演化中的关键作用。
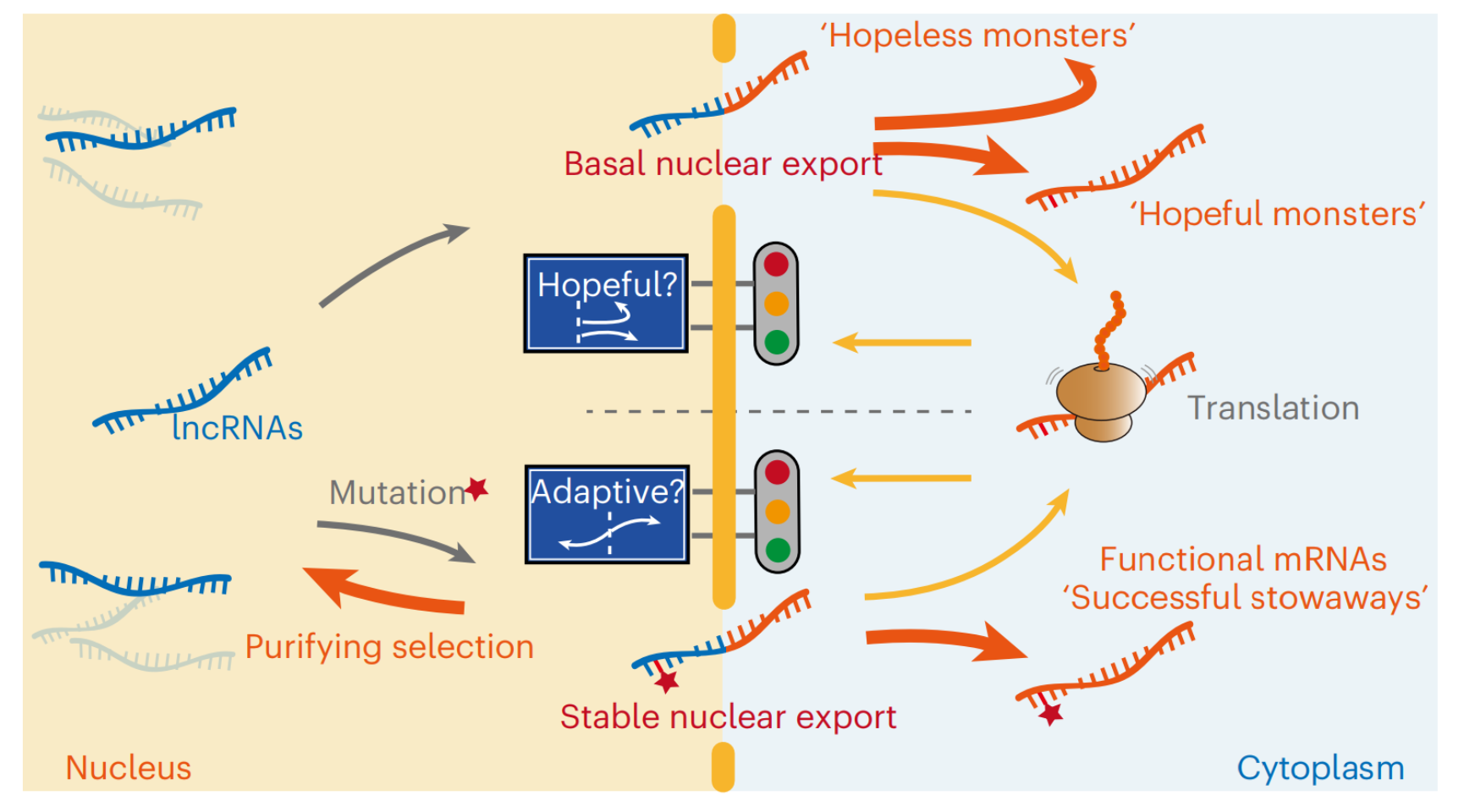
人类特有新基因的“偷渡者”起源模型
该研究发现,某些突变通过赋予其编码的RNA逃避细胞核的技能----翻译成蛋白质的关键一步----将看似无用的DNA序列转化为潜在基因。研究者强调了74个人类蛋白质基因,这些基因似乎均是以这种从头起源(de novoorigination)方式出现的----其中一半以上是在人类谱系从黑猩猩分支分离出来之后出现的。其中一些新基因可能在人类大脑的进化中发挥了作用----当这些新基因被添加到小鼠身上时,会使啮齿动物的大脑变得更大,更像人类。
美国匹兹堡大学进化生物学家Anne-Ruxandra Carvunis(未参与该研究)评论说: “这项工作是一个很大的进步,它表明从头基因(de novo)的诞生可能在人类大脑进化中发挥了作用。”

科学家们已经追踪了数十种人类特异性基因的诞生----其中一些基因被认为是帮助人类大脑进化(优于其他灵长类动物)的关键。
线索的出现
02
十年前,李川昀教授及其同事发现,一些人类蛋白质基因与恒河猴的DNA序列惊人地相似。在恒河猴体内,这些DNA序列被转录成长非编码RNA(lncRNA);然而,这些RNA(lncRNA)不产生蛋白质,也不具有任何其他明显目的。在当时,李和他的同事还无法弄清楚这些恒河猴的DNA片段究竟是在什么情况下才会变成人类体内的蛋白质编码基因。
幸运的是,解答上述疑问的线索出现了----李教授的博士后安妮发现许多lncRNA很难离开细胞核。研究人员使用复杂的计算机程序来识别mRNA脱离细胞核的蛋白质编码基因与产生不脱离细胞核的RNA的DNA序列之间的差异。该程序专注于称为U1元素的DNA片段:当转录成RNA时,会使链太粘而无法干净地逃逸;而在蛋白质编码基因中,这些元素具有使RNA粘性降低的突变。因此,为了使lncRNA逃离细胞核并将其指令传递给核糖体,亲本DNA(parental DNA)必须获得这些关键的U1突变,或者以某种方式使转录的部分完全从RNA链中切断。
“这完全有道理,” 西班牙德尔马医院医学研究所进化生物学家Maria Del Mar Albà评论道,“因为RNA是需要被翻译的,所以RNA首先需要进入细胞质----核糖体存在的地方。”
Carvunis表示:“这项工作表明,通过DNA序列的微妙变化,可能会产生深远影响的从头基因(de novo);但关于逃逸的lncRNA最终如何成为真正的基因,还有很多东西需要了解。”
“基因诞生有很多障碍,我希望这项工作将有助于激发更多的研究,以了解这些障碍是什么以及新兴基因如何克服它们。”(转化医学网360zhyx.com)
参考资料:
https://www.science.org/content/article/human-gene-linked-bigger-brains-was-born-seemingly-useless-dna
https://news.pku.edu.cn/jxky/034eeb039b9a4d3a9b126e07f6136495.htm
https://www.nature.com/articles/s41559-022-01925-6
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
摘自网址:http://www.360zhyx.com/home-research-index-rid-77596.shtml