

4月19日,江苏大学医学院张徐和南通肿瘤医院顾建美共同通讯在期刊《ADVANCED SCIENCE》上在线发表题为“M2 Tumor-Associated Macrophages-Derived Exosomal MALAT1 Promotes Glycolysis and Gastric Cancer Progression”的研究论文,研究人员发现M2 TAM分泌外泌体将 MALAT1 传递到胃癌细胞,其中 MALAT1 稳定了δ-连环蛋白并上调了HIF-1α的表达,导致糖酵解增强和胃癌进展。研究结果揭示了TME中M2 TAM和胃癌细胞之间的新相互作用,并提出了 MALAT1 在胃癌进展中的新功能。

https://onlinelibrary.wiley.com/doi/10.1002/advs.202309298
研究背景
01
胃癌是全球癌症相关死亡的主要原因之一。尽管最近在早期诊断和治疗方面取得了进展,但晚期和转移性疾病患者的生存率仍然很低。手术后转移的发生和治疗耐药性仍然是阻碍患者生存率提高的主要挑战。因此,更好地了解导致胃癌疾病进展的病理机制可能会导致设计更有效的治疗方法。
肿瘤微环境(TME)是一个复杂的生态系统,由不同的细胞群组成,包括肿瘤细胞、成纤维细胞和免疫细胞等,并积极参与肿瘤的发生和进展。肿瘤相关巨噬细胞(TAM)是存在于TME中的异质性髓样细胞群,通常分为M1和M2亚型。通过肿瘤的再教育过程,TAMs转变为促肿瘤M2表型,并与肿瘤细胞协同促进肿瘤生长和转移。先前研究表明,肿瘤细胞可以通过分泌炎性细胞因子和趋化因子、细胞外囊泡和肿瘤代谢物来诱导TAM的M2极化。反过来,M2 TAM通过促进肿瘤细胞增殖和EMT(上皮-间充质转化)、诱导肿瘤血管生成和转移前生态位的形成以及介导肿瘤免疫抑制来促进肿瘤生长和转移。因此,已经建议巨噬细胞靶向治疗策略与当前可用的方案进行补充和协同,以获得更好的癌症治疗。
研究发现
02
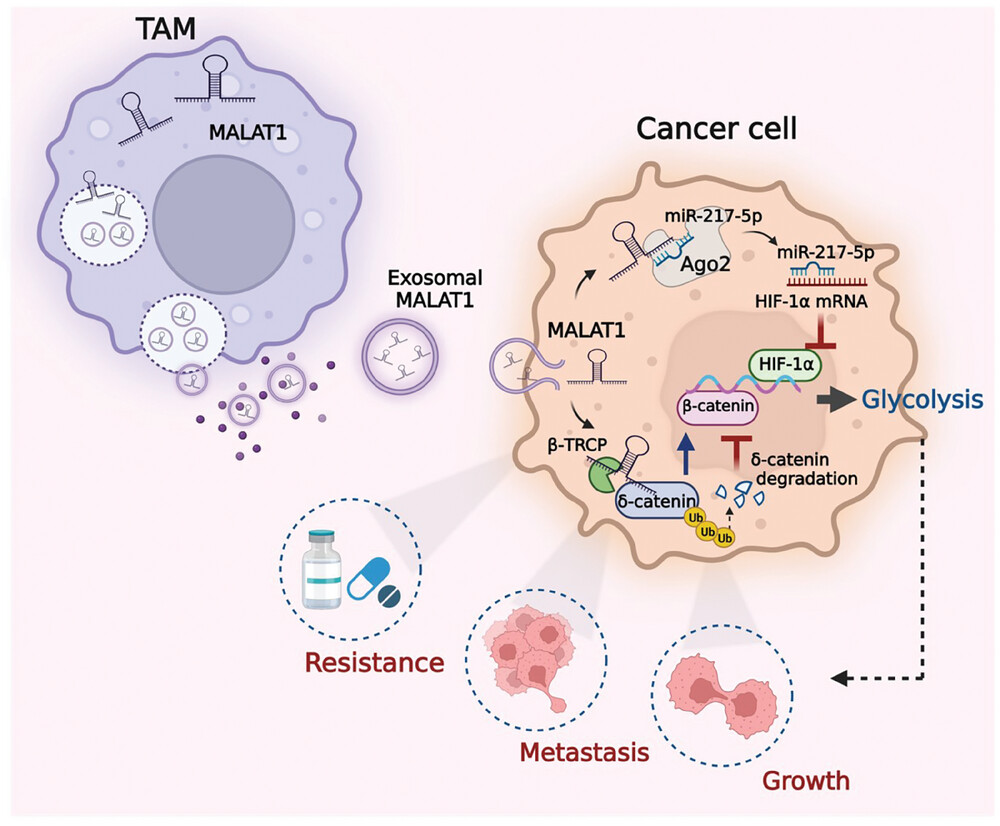
在研究中,M2 TAMs衍生的外泌体诱导胃癌细胞的有氧糖酵解,并以糖酵解依赖性方式增强其增殖、转移和化疗耐药性。经鉴定,MALAT1(转移相关肺腺癌转录本1)富集在M2 TAM外泌体中,并证实 MALAT1 通过外泌体从M2 TAM转移到胃癌细胞介导这种作用。机制上,MALAT1与δ-catenin蛋白相互作用,并通过β-TRCP抑制其泛素化和降解。此外,MALAT1 通过充当miR-217-5p的海绵上调 HIF-1α 表达。M2 TAM外泌体激活β-连环蛋白和HIF-1α信号通路共同导致胃癌细胞有氧糖酵解增强。最后,通过外泌体介导的siRNA递送对胃癌细胞和巨噬细胞中MALAT1的双靶点抑制显著抑制了胃癌的生长,并改善了小鼠肿瘤模型的化学敏感性。综上所述,这些结果表明,M2 TAMs衍生的外泌体通过MALAT1介导的糖酵解调节促进胃癌进展。这些发现为胃癌治疗提供了潜在的靶点。
研究结论
03
综上所述,研究人员发现M2 TAM分泌外泌体将 MALAT1 传递到胃癌细胞,其中 MALAT1 稳定了δ-连环蛋白并上调了HIF-1α的表达,导致糖酵解增强和胃癌进展。研究结果揭示了TME中M2 TAM和胃癌细胞之间的新相互作用,并提出了 MALAT1 在胃癌进展中的新功能。(转化医学网360zhyx.com)
参考资料:
https://onlinelibrary.wiley.com/doi/10.1002/advs.202309298
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
摘自网址:http://www.360zhyx.com/home-research-index-rid-79640.shtml